Page 14 - Cooper - La Célula (8ª Edición) - Marbán Libros S.L.
P. 14
12
412 Sección III • Estructura y función celulares Distribución y transporte de proteínas 413
(A) (B) Rab diferentes y se ha demostrado que funcionan en procesos específicos de
transporte de vesículas, con diferentes proteínas Rab que marcan diferentes
Lumen de Golgi Vesícula
Cargo Cubierta orgánulos y vesículas de transporte. Las proteínas Rab de la vesícula en el
estado activo de unión a GTP se unen a factores de unión a la membrana,
proporcionando el puente inicial entre las membranas diana y de la vesícu-
Arf Arf/GEF Proteína Receptor SNARE la. Los factores de anclaje también se unen a las proteínas de la cubierta, lo
adaptadora
que contribuye a su interacción con las vesículas.
Factor de El anclaje es seguido por la formación de complejos entre pares específi-
Rab
SNARE
anclaje
GDP GTP GTP GTP Diana cos de proteínas transmembrana llamadas SNARE en las membranas vesi-
culares y diana (ver Figura 12.32). Este emparejamiento de SNARE en la
vesícula y membranas diana proporciona la energía para impulsar la fusión
GTP GDP Clatrina de las bicapas de fosfolípidos. Las proteínas SNARE tienen un dominio en
espiral central largo como el que se encuentra en las láminas nucleares (ver
Figura 11.4). Al igual que en las láminas, este dominio se une fuertemente a
otros dominios en espiral y, en efecto, une las SNARE de las membranas de
vesícula y diana, poniendo las dos membranas en contacto directo y dando
Dinamina
lugar a la fusión de las bicapas lipídicas.
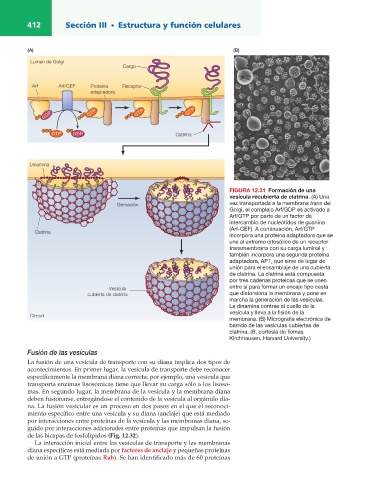
FIGURA 12.31 Formación de una Lisosomas
vesícula recubierta de clatrina. (A) Una Objetivos de aprendizaje
Gemación vez transportada a la membrana trans del Eliminación
Golgi, el complejo Arf/GDP es activado a de la cubierta Deberías ser capaz de:
Arf/GTP por parte de un factor de • Describir la función de los lisosomas.
intercambio de nucleótidos de guanina
(Arf-GEF). A continuación, Arf/GTP • Explicar cómo se forman los lisosomas.
Clatrina
incorpora una proteína adaptadora que se • Resumir el proceso de autofagia.
une al extremo citosólico de un receptor SNARE
transmembrana con su carga luminal y
también incorpora una segunda proteína Los lisosomas son orgánulos rodeados de membrana que contienen una
adaptadora, AP1, que sirve de lugar de serie de enzimas capaces de degradar todas las clases de polímeros biológi-
unión para el ensamblaje de una cubierta cos —proteínas, ácidos nucleicos, carbohidratos y lípidos—. Los lisosomas
de clatrina. La clatrina está compuesta Fusión de funcionan como el sistema digestivo de la célula, sirviendo tanto para de-
membranas
por tres cadenas proteicas que se unen gradar el material captado del exterior de la célula como para digerir los
Vesícula entre sí para formar un encaje tipo cesta componentes obsoletos de la propia célula. En su forma más sencilla, los li-
cubierta de clatrina que distorsiona la membrana y pone en
marcha la generación de las vesículas. sosomas se observan como vacuolas esféricas densas, pero pueden exhibir
La dinamina contrae el cuello de la diversidad de tamaños y de formas en función de los distintos materiales
vesícula y lleva a la fisión de la que hayan captado (Fig. 12.33). Por tanto, los lisosomas representan orgá-
Citosol
membrana. (B) Micrografía electrónica de nulos morfológicamente diversos definidos por la función común de degra-
barrido de las vesículas cubiertas de dar material intracelular.
clatrina. (B, cortesía de Tomas FIGURA 12.32 Anclaje y fusión de
Kirchhausen, Harvard University.) las vesículas. Una proteína Rab de la
membrana de la vesícula se une a un Hidrolasas lisosómicas ácidas
Fusión de las vesículas factor de anclaje asociado con la Los lisosomas contienen alrededor de 60 enzimas degradativas diferentes
La fusión de una vesícula de transporte con su diana implica dos tipos de membrana diana. A continuación tiene que pueden hidrolizar proteínas, ADN, ARN, polisacáridos y lípidos. Las
acontecimientos. En primer lugar, la vesícula de transporte debe reconocer lugar la formación de complejos entre mutaciones en los genes que codifican estas proteínas son responsables de
SNARE en la vesícula y las
específicamente la membrana diana correcta; por ejemplo, una vesícula que membranas diana. Los dominios más de 30 enfermedades congénitas humanas diferentes, que se denominan
transporta enzimas lisosómicas tiene que llevar su carga sólo a los lisoso- arrollados de los SNARE se unen en enfermedades de depósito lisosómico, ya que el material no degradado se
mas. En segundo lugar, la membrana de la vesícula y la membrana diana cremallera entre sí, con lo que acercan acumula en los lisosomas de los individuos afectados. La mayoría de estas
deben fusionarse, entregándose el contenido de la vesícula al orgánulo dia- la vesícula y las membranas, de enfermedades se deben a deficiencias en una única enzima lisosómica. Por
na. La fusión vesicular es un proceso en dos pasos en el que el reconoci- manera que las membranas se ejemplo, la enfermedad de Gaucher (la alteración más común) se debe a
miento específico entre una vesícula y su diana (anclaje) que está mediado fusionan. una mutación en el gen que codifica una enzima lisosómica requerida para
por interacciones entre proteínas de la vesícula y las membranas diana, se- la degradación de los glicolípidos (véase Medicina Molecular). Una excep-
guido por interacciones adicionales entre proteínas que impulsan la fusión ción curiosa es la enfermedad celular-I, que se debe a una eficiencia en la
de las bicapas de fosfolípidos (Fig. 12.32). enzima que cataliza el primer paso en el marcaje de las enzimas lisosómicas
La interacción inicial entre las vesículas de transporte y las membranas Los lisosomas contienen enzimas con manosa-6-fosfato en el aparato de Golgi (véase Fig. 12.24). El resultado
Cooper The Cell 7e, Sinauer/ASM
Cooper_The Cell 8e que degradan proteínas y otras es una alteración generalizada en la incorporación de las enzimas lisosómi-
diana específicas está mediada por factores de anclaje y pequeñas proteínas
Figure# 11.37 DMG#1137
Sinauer macromoléculas. cas a los lisosomas.
de unión a GTP (proteínas Rab). Se han identificado más de 60 proteínas
Dragon y Media Group 07/28/17
Figure# 12.31 05/16/18 Dragonfly Media Group
Cooper_Celula_8Ed_22,5x29_Montado_2021.indd 412 22/7/21 12:43
12_Cooper_Celula_Ed_8Ed_210x280_2021.indd 412 22/7/21 11:54 12_Cooper_Celula_Ed_8Ed_210x280_2021.indd 413 22/7/21 11:54